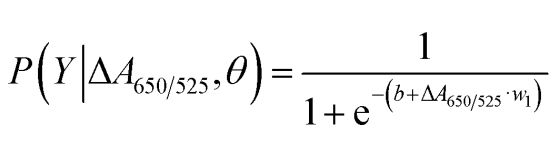Tidlig opdagelse af kræft baseret på flydende biopsi er en ny retning inden for kræftdetektion og -diagnose, som det amerikanske National Cancer Institute har foreslået i de senere år med det formål at opdage tidlig kræft eller endda præcancerøse læsioner. Det har været bredt anvendt som en ny biomarkør til tidlig diagnose af forskellige maligniteter, herunder lungekræft, gastrointestinale tumorer, gliomer og gynækologiske tumorer.
Fremkomsten af platforme til at identificere biomarkører i metyleringslandskabet (Methylscape) har potentiale til at forbedre eksisterende tidlig screening for kræft betydeligt og bringe patienter i det tidligst behandlingsbare stadie.
For nylig har forskere udviklet en simpel og direkte sensorplatform til detektion af methyleringslandskaber baseret på cysteamin-dekorerede guldnanopartikler (Cyst/AuNP'er) kombineret med en smartphone-baseret biosensor, der muliggør hurtig tidlig screening af en bred vifte af tumorer. Tidlig screening for leukæmi kan udføres inden for 15 minutter efter DNA-ekstraktion fra en blodprøve med en nøjagtighed på 90,0 %. Artiklens titel er Hurtig detektion af kræft-DNA i humant blod ved hjælp af cysteamin-kappede AuNP'er og en maskinlæringsaktiveret smartphone.
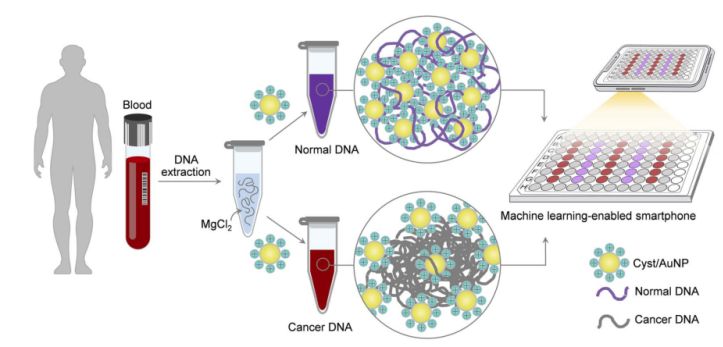
Figur 1. En simpel og hurtig sensorplatform til kræftscreening via cyste/AuNP-komponenter kan opnås i to enkle trin.
Dette er vist i figur 1. Først blev en vandig opløsning brugt til at opløse DNA-fragmenterne. Cyst/AuNP'er blev derefter tilsat den blandede opløsning. Normalt og malignt DNA har forskellige methyleringsegenskaber, hvilket resulterer i DNA-fragmenter med forskellige selvsamlingsmønstre. Normalt DNA aggregerer løst og aggregerer til sidst Cyst/AuNP'er, hvilket resulterer i Cyst/AuNP'ers rødforskudte natur, således at en farveændring fra rød til lilla kan observeres med det blotte øje. I modsætning hertil fører den unikke methyleringsprofil af kræft-DNA til produktion af større klynger af DNA-fragmenter.
Billeder af 96-brønds plader blev taget med et smartphonekamera. Kræft-DNA blev målt af en smartphone udstyret med maskinlæring sammenlignet med spektroskopi-baserede metoder.
Kræftscreening i rigtige blodprøver
For at udvide anvendeligheden af sensorplatformen anvendte forskerne en sensor, der med succes kunne skelne mellem normalt og kræftfremkaldende DNA i rigtige blodprøver. Metyleringsmønstre på CpG-steder regulerer epigenetisk genekspression. I næsten alle kræfttyper er der observeret vekslende ændringer i DNA-metylering og dermed i ekspressionen af gener, der fremmer tumordannelse.
Som model for andre kræftformer forbundet med DNA-methylering brugte forskerne blodprøver fra leukæmipatienter og raske kontrolpersoner til at undersøge effektiviteten af methyleringslandskabet i differentieringen af leukæmiske kræftformer. Denne methyleringslandskabsbiomarkør overgår ikke kun eksisterende hurtige leukæmiscreeningsmetoder, men demonstrerer også muligheden for at udvide til tidlig påvisning af en bred vifte af kræftformer ved hjælp af dette enkle og ligetil assay.
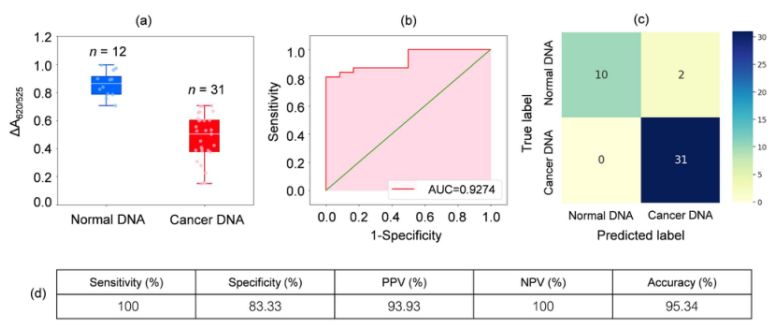
DNA fra blodprøver fra 31 leukæmipatienter og 12 raske individer blev analyseret. Som vist i boksplottet i figur 2a var den relative absorbans af kræftprøverne (ΔA650/525) lavere end absorbansen for DNA fra normale prøver. Dette skyldtes primært den forbedrede hydrofobicitet, der førte til tæt aggregering af kræft-DNA, hvilket forhindrede aggregering af Cyst/AuNP'er. Som et resultat blev disse nanopartikler fuldstændigt dispergeret i de ydre lag af kræftaggregaterne, hvilket resulterede i en forskellig dispersion af Cyst/AuNP'er adsorberet på normale og kræft-DNA-aggregater. ROC-kurver blev derefter genereret ved at variere tærsklen fra en minimumsværdi på ΔA650/525 til en maksimumsværdi.
Figur 2.(a) Relative absorbansværdier af cyste/AuNP-opløsninger, der viser tilstedeværelsen af normalt (blåt) og kræft- (rødt) dna under optimerede forhold.
(DA650/525) af boksplot; (b) ROC-analyse og evaluering af diagnostiske tests. (c) Forvirringsmatrix til diagnosticering af normale patienter og kræftpatienter. (d) Sensitivitet, specificitet, positiv prædiktiv værdi (PPV), negativ prædiktiv værdi (NPV) og nøjagtighed af den udviklede metode.
Som vist i figur 2b udviste arealet under ROC-kurven (AUC = 0,9274) opnået for den udviklede sensor høj følsomhed og specificitet. Som det kan ses af boksplottet, er det laveste punkt, der repræsenterer den normale DNA-gruppe, ikke godt adskilt fra det højeste punkt, der repræsenterer kræft-DNA-gruppen; derfor blev logistisk regression brugt til at differentiere mellem de normale grupper og kræftgrupperne. Givet et sæt uafhængige variabler estimerer den sandsynligheden for, at en begivenhed indtræffer, såsom en kræft- eller normal gruppe. Den afhængige variabel ligger mellem 0 og 1. Resultatet er derfor en sandsynlighed. Vi bestemte sandsynligheden for kræftidentifikation (P) baseret på ΔA650/525 som følger.
hvor b=5,3533,w1=-6,965. For stikprøveklassificering indikerer en sandsynlighed på mindre end 0,5 en normal stikprøve, mens en sandsynlighed på 0,5 eller højere indikerer en kræftprøve. Figur 2c viser den forvirringsmatrice, der blev genereret fra "leave-it-alone"-krydsvalideringen, som blev brugt til at validere klassificeringsmetodens stabilitet. Figur 2d opsummerer den diagnostiske testevaluering af metoden, herunder sensitivitet, specificitet, positiv prædiktiv værdi (PPV) og negativ prædiktiv værdi (NPV).
Smartphone-baserede biosensorer
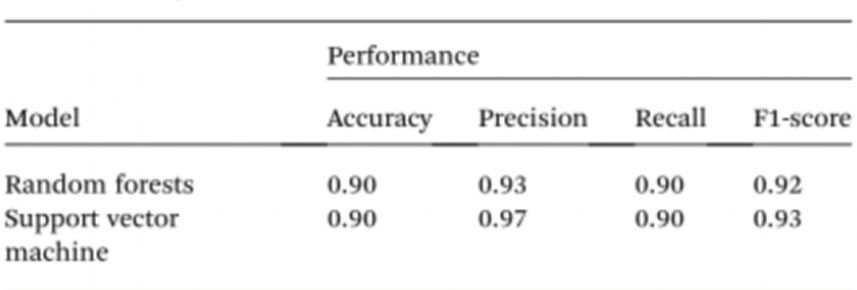
For yderligere at forenkle prøvetestning uden brug af spektrofotometre brugte forskerne kunstig intelligens (AI) til at fortolke opløsningens farve og skelne mellem normale og kræftramte individer. På baggrund af dette blev computervision brugt til at oversætte farven på Cyst/AuNPs-opløsningen til normalt DNA (lilla) eller kræft-DNA (rødt) ved hjælp af billeder af 96-brøndsplader taget gennem et mobiltelefonkamera. Kunstig intelligens kan reducere omkostninger og forbedre tilgængeligheden i forbindelse med fortolkning af farven på nanopartikelopløsninger og uden brug af optisk hardware eller smartphone-tilbehør. Endelig blev to maskinlæringsmodeller, herunder Random Forest (RF) og Support Vector Machine (SVM), trænet til at konstruere modellerne. Både RF- og SVM-modellerne klassificerede korrekt prøverne som positive og negative med en nøjagtighed på 90,0 %. Dette tyder på, at brugen af kunstig intelligens i mobiltelefonbaseret biosensing er fuldt ud mulig.
Figur 3. (a) Målklasse for opløsningen registreret under forberedelsen af prøven til billedoptagelsestrinnet. (b) Eksempelbillede taget under billedoptagelsestrinnet. (c) Farveintensitet af cyste/AuNP-opløsningen i hver brønd på 96-brøndspladen ekstraheret fra billedet (b).
Ved hjælp af cyster/aunp'er har forskere med succes udviklet en simpel sensorplatform til detektion af metyleringslandskaber og en sensor, der er i stand til at skelne normalt DNA fra kræft-DNA, når der anvendes rigtige blodprøver til leukæmiscreening. Den udviklede sensor viste, at DNA ekstraheret fra rigtige blodprøver var i stand til hurtigt og omkostningseffektivt at detektere små mængder kræft-DNA (3 nM) hos leukæmipatienter på 15 minutter og viste en nøjagtighed på 95,3 %. For yderligere at forenkle prøvetestning ved at eliminere behovet for et spektrofotometer blev maskinlæring brugt til at fortolke opløsningens farve og skelne mellem normale og kræftramte individer ved hjælp af et mobiltelefonfotografi, og en nøjagtighed kunne også opnås på 90,0 %.
Reference: DOI: 10.1039/d2ra05725e
Opslagstidspunkt: 18. feb. 2023
 中文网站
中文网站