Nat Med | En multi-omics-tilgang til kortlægning af det integrerede tumor-, immun- og mikrobielle landskab i kolorektal cancer afslører mikrobiomets interaktion med immunsystemet
Selvom biomarkører for primær tyktarmskræft er blevet undersøgt grundigt i de senere år, er nuværende kliniske retningslinjer kun baseret på stadieinddeling af tumor-lymfeknude-metastaser og detektion af DNA-mismatch-reparationsdefekter (MMR) eller mikrosatellitinstabilitet (MSI) (ud over standard patologitest) for at bestemme behandlingsanbefalinger. Forskere har bemærket en manglende sammenhæng mellem genekspressionsbaserede immunresponser, mikrobielle profiler og tumorstroma i Cancer Genome Atlas (TCGA) kolorektal cancer-kohorten og patientoverlevelse.
Efterhånden som forskningen er skredet frem, er det rapporteret, at kvantitative karakteristika ved primær kolorektal cancer, herunder kræftens cellulære, immunologiske, stromale eller mikrobielle natur, korrelerer signifikant med kliniske resultater, men der er stadig begrænset forståelse af, hvordan deres interaktioner påvirker patientresultaterne.
For at dissekere forholdet mellem fænotypisk kompleksitet og resultat har et forskerhold fra Sidra Institute of Medical Research i Qatar for nylig udviklet og valideret en integreret score (mICRoScore), der identificerer en gruppe patienter med gode overlevelsesrater ved at kombinere mikrobiomkarakteristika og immunafstødningskonstanter (ICR). Holdet udførte en omfattende genomisk analyse af friskfrosne prøver fra 348 patienter med primær kolorektal cancer, herunder RNA-sekventering af tumorer og matchet sundt kolorektalt væv, hel exom-sekventering, dyb T-cellereceptor- og 16S bakteriel rRNA-gensekventering, suppleret med hel tumorgenomsekventering for yderligere at karakterisere mikrobiomet. Undersøgelsen blev offentliggjort i Nature Medicine som "Et integreret tumor-, immun- og mikrobiomatlas af colon cancer".

Artikel udgivet i Nature Medicine
AC-ICAM Oversigt
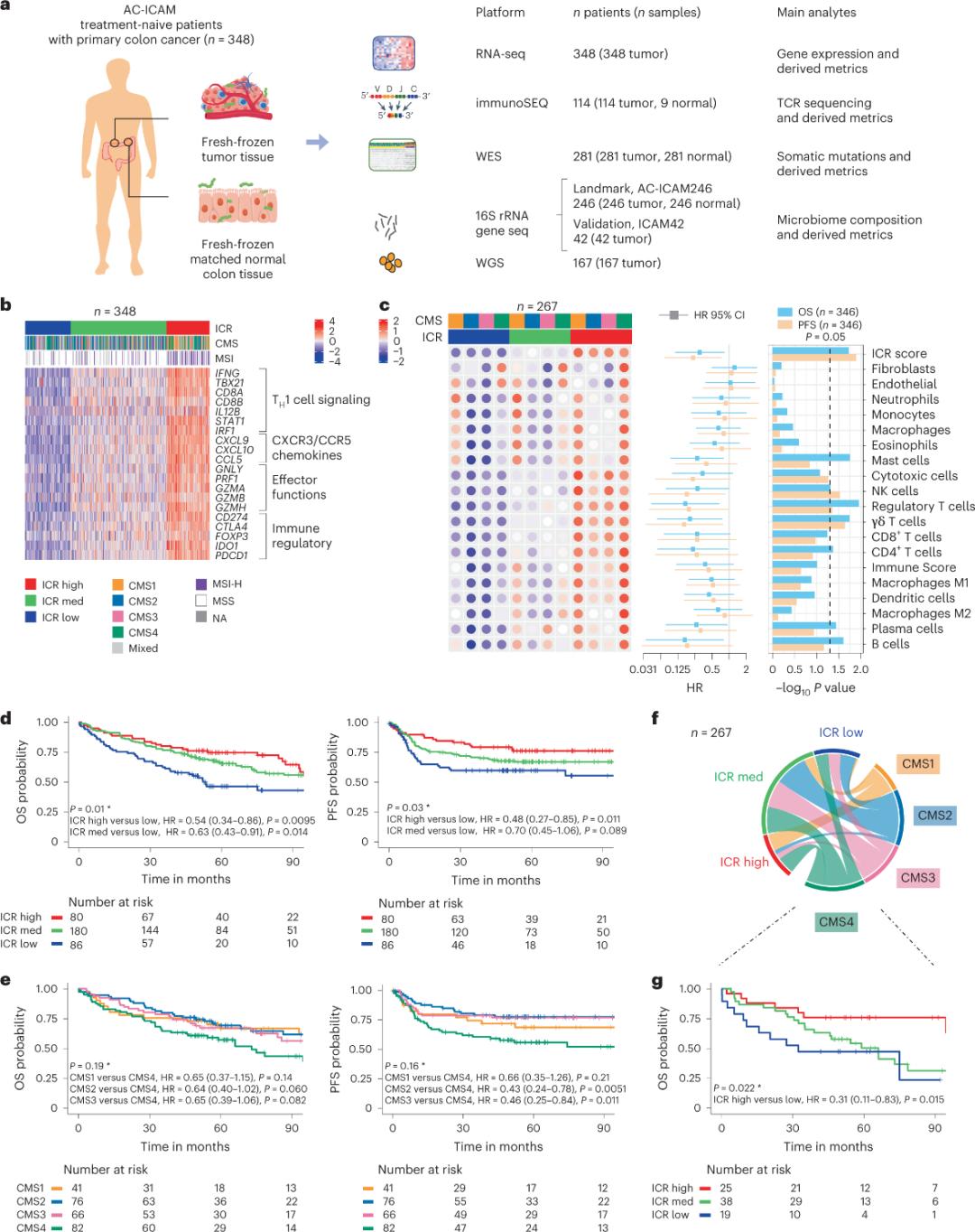
Forskerne brugte en ortogonal genomisk platform til at analysere friske, frosne tumorprøver og matchede tilstødende sundt tyktarmsvæv (tumor-normale par) fra patienter med en histologisk diagnose af tyktarmskræft uden systemisk behandling. Baseret på hel-eksom-sekventering (WES), RNA-sekvenseringsdatakvalitetskontrol og screening efter inklusionskriterier blev genomiske data fra 348 patienter bevaret og brugt til downstream-analyse med en median opfølgningstid på 4,6 år. Forskerholdet kaldte denne ressource Sidra-LUMC AC-ICAM: Et kort og en vejledning til immun-kræft-mikrobiominteraktioner (Figur 1).
Molekylær klassificering ved hjælp af ICR
Ved at indsamle et modulært sæt af immungenetiske markører til kontinuerlig kræftimmunovervågning, kaldet immunafstødningskonstanten (ICR), optimerede forskerholdet ICR ved at kondensere den til et panel med 20 gener, der dækker forskellige kræfttyper, herunder melanom, blærekræft og brystkræft. ICR er også blevet forbundet med immunterapirespons i en række forskellige kræfttyper, herunder brystkræft.
Først validerede forskerne ICR-signaturen af AC-ICAM-kohorten ved hjælp af en ICR-genbaseret koklassificeringsmetode til at klassificere kohorten i tre klynger/immunundertyper: høj ICR (varme tumorer), medium ICR og lav ICR (kolde tumorer) (Figur 1b). Forskerne karakteriserede den immune tilbøjelighed forbundet med konsensus molekylære undertyper (CMS), en transkriptombaseret klassificering af tyktarmskræft. CMS-kategorierne omfattede CMS1/immun, CMS2/kanonisk, CMS3/metabolisk og CMS4/mesenkymal. Analyse viste, at ICR-scorer var negativt korreleret med visse kræftcelleveje i alle CMS-undertyper, og positive korrelationer med immunsuppressive og stromale relaterede veje blev kun observeret i CMS4-tumorer.
I alle CMS var forekomsten af naturlige dræberceller (NK) og T-celle-subgrupper højest i ICR-højimmune subtyper, med større variation i andre leukocyt-subgrupper (Figur 1c). ICR-immune subtyper havde forskellig OS og PFS, med en progressiv stigning i ICR fra lav til høj (Figur 1d), hvilket validerer ICR's prognostiske rolle i kolorektal cancer.
Figur 1. AC-ICAM-studiedesign, immunrelateret gensignatur, immun- og molekylære subtyper og overlevelse.
ICR indfanger tumorberigede, klonalt amplificerede T-celler
Kun et mindretal af T-celler, der infiltrerer tumorvæv, er rapporteret at være specifikke for tumorantigener (mindre end 10%). Derfor betegnes størstedelen af intra-tumor T-celler som bystander T-celler (bystander T-celler). Den stærkeste korrelation med antallet af konventionelle T-celler med produktive TCR'er blev observeret i stromale celle- og leukocyt-subpopulationer (detekteret ved RNA-seq), hvilket kan bruges til at estimere T-celle-subpopulationer (Figur 2a). I ICR-klyngerne (samlet og CMS-klassifikation) blev den højeste klonalitet af immune SEQ TCR'er observeret i ICR-høj og CMS-subtype CMS1/immungrupperne (Figur 2c), med den højeste andel af ICR-høje tumorer. Ved at bruge hele transkriptomet (18.270 gener) var seks ICR-gener (IFNG, STAT1, IRF1, CCL5, GZMA og CXCL10) blandt de ti største gener, der var positivt associeret med TCR-immun SEQ-klonalitet (Figur 2d). ImmunoSEQ TCR-klonalitet korrelerede stærkere med de fleste ICR-gener end de korrelationer, der blev observeret ved hjælp af tumorresponsive CD8+ markører (Figur 2f og 2g). Afslutningsvis antyder ovenstående analyse, at ICR-signaturen indfanger tilstedeværelsen af tumorberigede, klonalt amplificerede T-celler og kan forklare dens prognostiske implikationer.
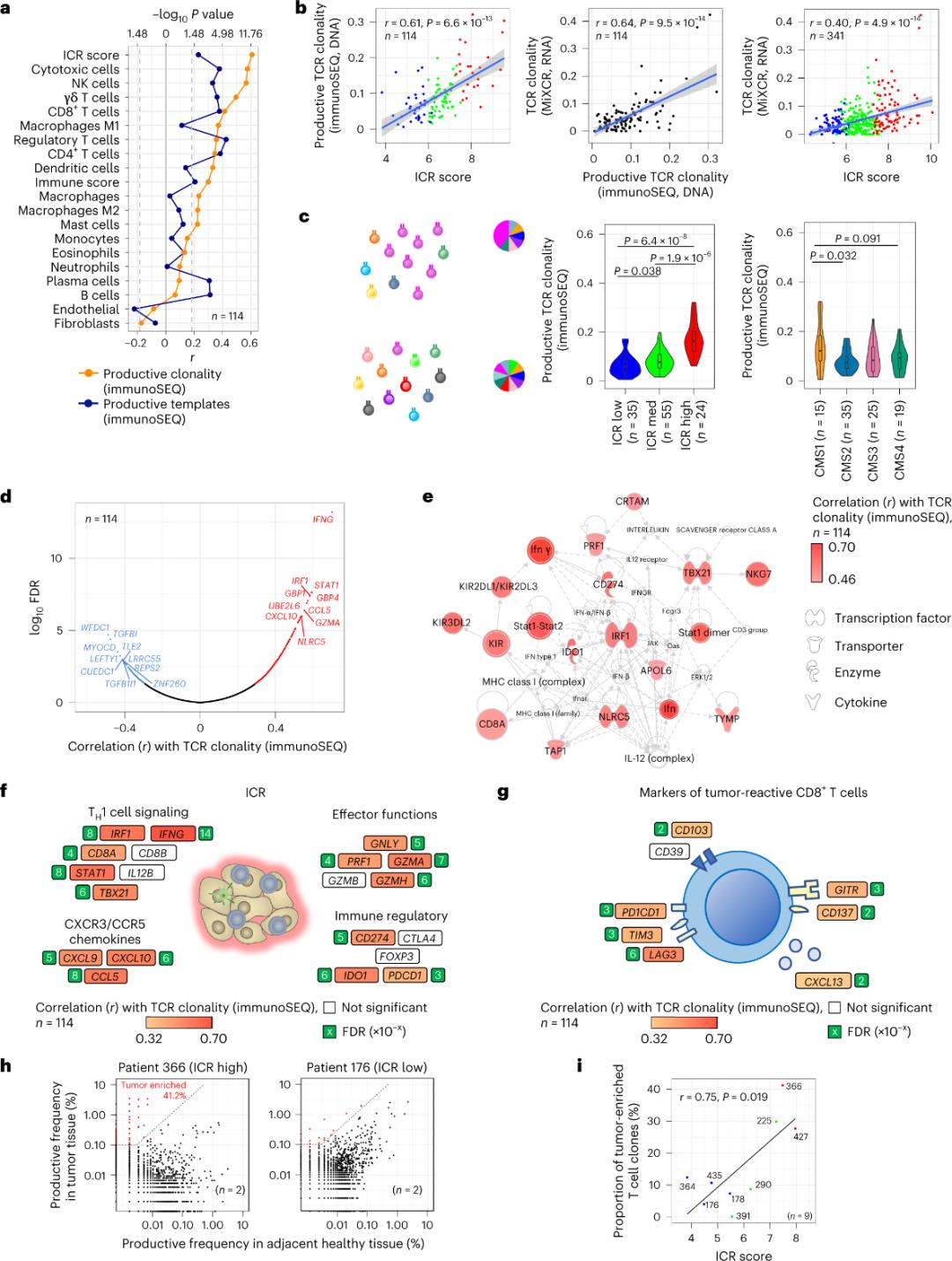
Figur 2. TCR-metrikker og korrelation med immunrelaterede gener, immun- og molekylære subtyper.
Mikrobiomsammensætning i sundt og tyktarmskræftvæv
Forskerne udførte 16S rRNA-sekventering ved hjælp af DNA ekstraheret fra matchet tumor og sundt tyktarmsvæv fra 246 patienter (figur 3a). Til validering analyserede forskerne yderligere 16S rRNA-gensekventeringsdata fra yderligere 42 tumorprøver, der ikke havde matchet normalt DNA tilgængeligt til analyse. Først sammenlignede forskerne den relative floraforekomst mellem matchede tumorer og sundt tyktarmsvæv. Clostridium perfringens var signifikant forøget i tumorerne sammenlignet med de sunde prøver (figur 3a-3d). Der var ingen signifikant forskel i alfa-diversitet (diversitet og forekomst af arter i en enkelt prøve) mellem tumor- og sunde prøver, og en beskeden reduktion i mikrobiel diversitet blev observeret i tumorer med høj ICR i forhold til tumorer med lav ICR.
For at detektere klinisk relevante sammenhænge mellem mikrobielle profiler og kliniske resultater, sigtede forskerne mod at bruge 16S rRNA-gensekvenseringsdata til at identificere mikrobiomfunktioner, der forudsiger overlevelse. Ved AC-ICAM246 kørte forskerne en OS Cox-regressionsmodel, der udvalgte 41 funktioner med koefficienter, der ikke var nul (forbundet med differentiel dødelighedsrisiko), kaldet MBR-klassifikatorer (Figur 3f).
I denne træningskohorte (ICAM246) var en lav MBR-score (MBR < 0, lav MBR) forbundet med en signifikant lavere risiko for død (85%). Forskerne bekræftede sammenhængen mellem lav MBR (risiko) og forlænget OS i to uafhængigt validerede kohorter (ICAM42 og TCGA-COAD). (Figur 3) Undersøgelsen viste en stærk korrelation mellem endogastriske kokker og MBR-scorer, som var ens i tumor- og sundt tyktarmsvæv.
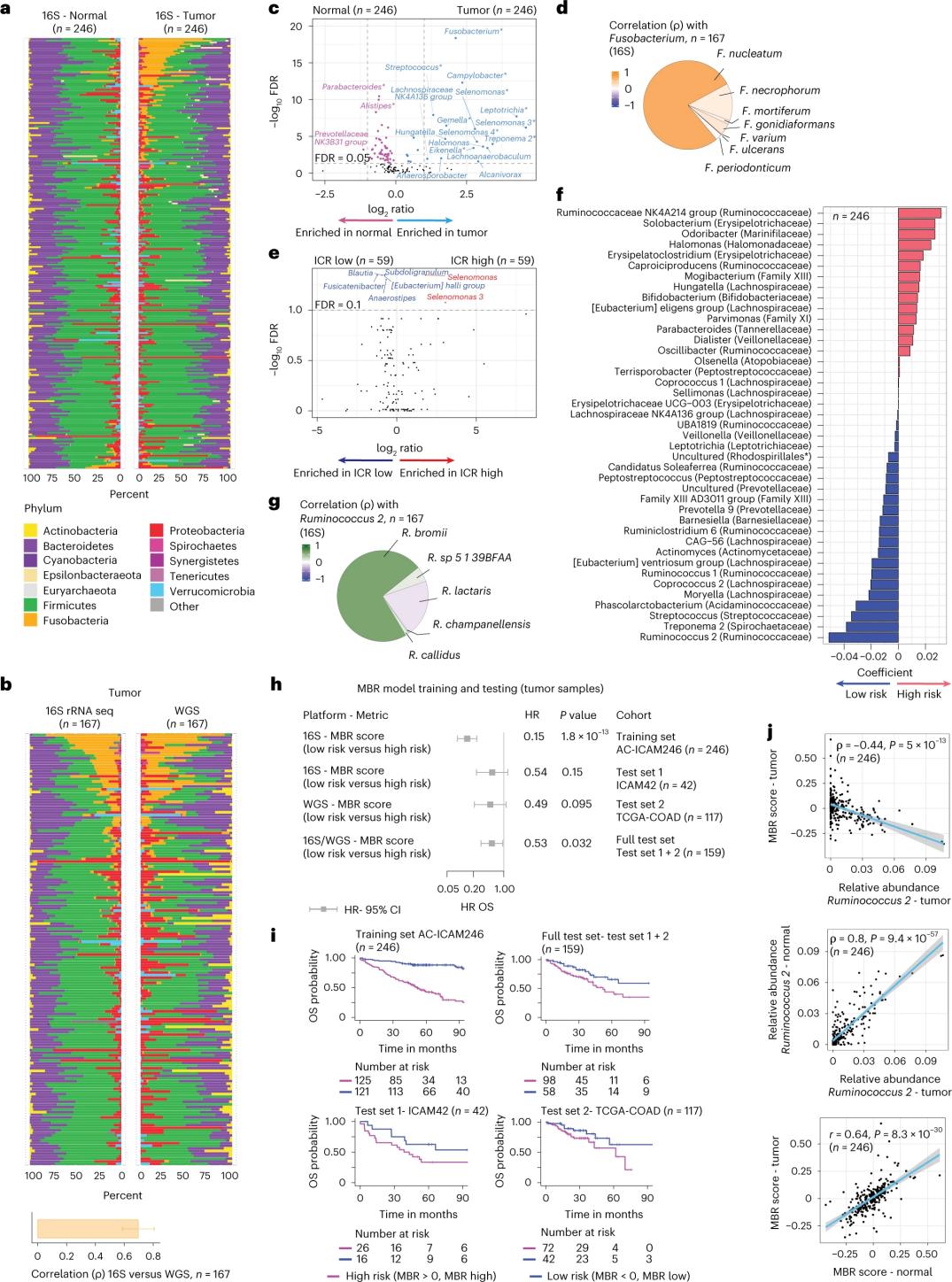
Figur 3. Mikrobiom i tumor og sundt væv og forholdet mellem ICR og patientoverlevelse.
Konklusion
Den multi-omics-tilgang, der anvendes i dette studie, muliggør grundig detektion og analyse af den molekylære signatur af immunresponset i kolorektal cancer og afslører interaktionen mellem mikrobiomet og immunsystemet. Dyb TCR-sekventering af tumor- og sundt væv afslørede, at den prognostiske effekt af ICR kan skyldes dens evne til at indfange tumorberigede og muligvis tumorantigenspecifikke T-cellekloner.
Ved at analysere tumormikrobiomsammensætningen ved hjælp af 16S rRNA-gensekventering i AC-ICAM-prøver identificerede teamet en mikrobiomsignatur (MBR-risikoscore) med stærk prognostisk værdi. Selvom denne signatur var afledt af tumorprøver, var der en stærk korrelation mellem sund kolorektum og tumor-MBR-risikoscore, hvilket tyder på, at denne signatur kan indfange patienternes tarmmikrobiomsammensætning. Ved at kombinere ICR- og MBR-scorerne var det muligt at identificere og validere en multiomisk studentbiomarkør, der forudsiger overlevelse hos patienter med tyktarmskræft. Studiets multiomiske datasæt giver en ressource til bedre at forstå tyktarmskræftbiologi og hjælpe med at opdage personlige terapeutiske tilgange.
Opslagstidspunkt: 15. juni 2023
 中文网站
中文网站